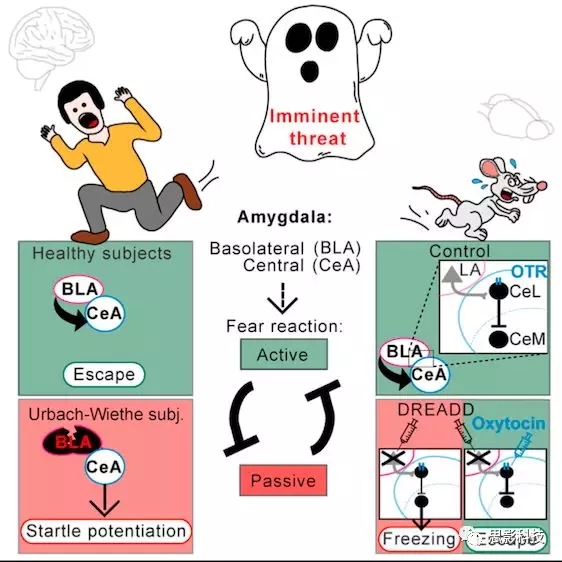
来自荷兰乌得勒支大学的David Terburg等人在Cell上发文,其团队研究发现,在即将发生威胁的实验前提下,通过激活中央杏仁核(CeA)途径,啮齿动物和人类的基底外侧杏仁核(BLA)对控制【主动执行逃避反应措施而不是被动地停滞行为】的过程起关键作用。文章选择局灶性双侧钙化的人群(具有BLA损伤,患有Urbach-Wiethe病),令其执行“威胁逃逸任务”,同时结合结构和功能性神经影像学技术,在人类受试者中搜索特定区域的活动变化。为进一步评估BLA是否对即将发生的威胁响应起作用,文章将人体实验转化为啮齿动物模型,选用具有化学遗传BLA神经元沉默的啮齿动物进行神经生物学实验。实验发现,当啮齿动物和人类面临迫在眉睫的威胁时,BLA对于快速逃避行为的选择和执行至关重要。实验发现了BLA通过激活特定一组CeA神经元,对即将来临的威胁实现快速逃逸反应的机制。该研究结果具有基础和临床相关性,这种机制应用于临床病理性恐惧和焦虑具有更深入的适用性,对人类和啮齿动物的进一步生物行为研究是至关重要的。
关键词:基底外侧杏仁核;中央杏仁核;Urbach-Wiethe病;快速逃避行为机制
啮齿动物研究已发现基底外侧杏仁核(BLA)和中央杏仁核(CeA)是如何控制防御行为,但是这些发现机制需与人类防御行为对应。本文将具有自然选择性的双侧BLA病变的人群与具有化学遗传的BLA神经元沉默的大鼠进行比较。结果发现,在物种间,BLA在暴露于迫在眉睫但无法逃避的威胁期间选择主动逃逸,而不是被动停滞的过程中起着重要作用(Timm调节)。与对照组相比,BLA损伤的人表现出惊恐增强,同时BLA沉默的大鼠表现出惊恐情绪增强、停滞和逃避动作减弱的行为。人体神经影像学表明,BLA通过CeA抑制脑干,降低了被动防御反应。实际上,Timm调节将BLA投射加强到抑制性CeA途径上,且该途径的药理学激活弥补了BLA沉默大鼠中缺乏的Timm反应。文章数据揭示了BLA如何通过CeA自适应地调节逃避行为以应对迫在眉睫的威胁,并且该机制在啮齿动物和人类中的进化是保守的。
人类研究结果
(一)钙化发生于人类双侧BLA区
本文研究者共选用5个UWD受试者,首先获得了每一个受试者的高分辨率T2加权MRI图像,使用MRI概率映射方法,能够量化每个杏仁核子区域的细胞构造钙化的结构-概率图。在每一个UWD受试者中,发现双侧钙化局限于BLA,而不影响CeA区域(图1)。
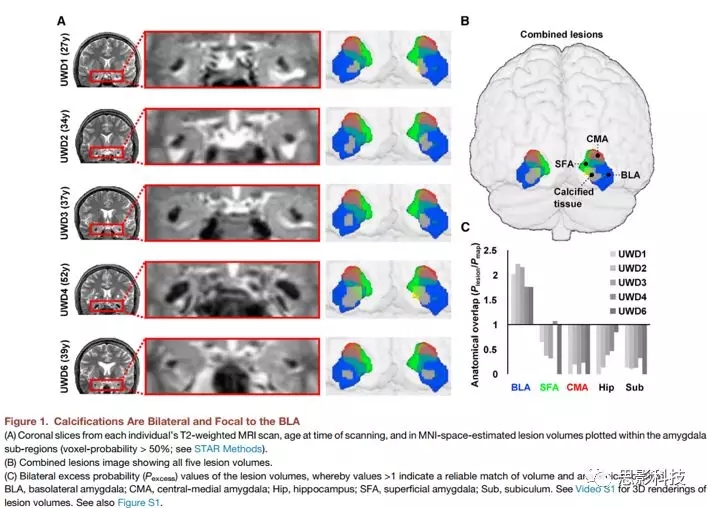
图1双侧BLA钙化
(二)BLA损伤导致潜在威胁增长至迫在眉睫的威胁
作者将UWD受试者与健康对照(HC)组(性别,年龄,智商和社会经济环境匹配)进行比较,在实验环境中动态改变威胁和逃避可能性。采用“威胁逃逸任务”(TET)”,指的是通过厌恶刺激(对手腕的电击),当视觉刺激明显接近时(屏幕尺寸增大,见图S1),可以通过按下按钮来避免这种刺激。具体指:
(1)“攻击”发生在“远距离”威胁之下(小型视觉刺激=震惊容易避免);
(2)“迫在眉睫”的威胁(中等大小=由于在线个人调整时间而有50%概率可以避免的震动);
(3)“不可避免的”威胁(全尺寸=震惊不可避免)。
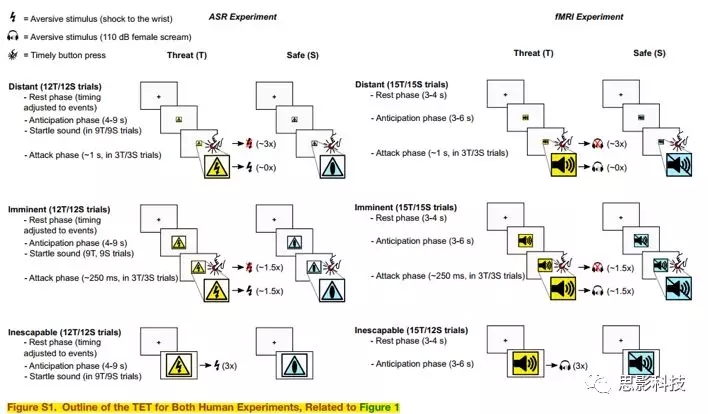
图S1针对人类的威胁逃逸任务(TET)实验
作者在实验期间进行眼轮匝肌眼肌的肌电图测量了声学触发的眨眼惊恐反射(ASR)(图2B),作为被动威胁反应的读数。与安全条件相比,ASR通常在不可避免的威胁中得到加强,因此,作者比较了威胁实验和安全试验之间的ASR(图2A)。
实验结果
在健康对照组中,伴随越来越多的威胁(遥远/迫在眉睫/不可避免),引起ASR与全等安全条件相比的增强(图2C)。但是,针对暴露在迫在眉睫的威胁期间,即必须抑制防御性停滞反应产生成功逃脱的模式下,健康对照和BLA损伤的受试者之间出现了显著差异。
在BLA损伤的受试者中,ASR通过迫在眉睫的威胁加强到与不可避免的威胁相同的水平,而这种即将发生的威胁的增强在健康对照中显著降低(图2C)。这为BLA损伤的人类受试者和健康对照之间的对强烈惊吓的不同反应这种显著差异,提供了重要证据,即在准备快速逃离威胁时,功能性BLA抑制反射方式与被动防御行为相关。
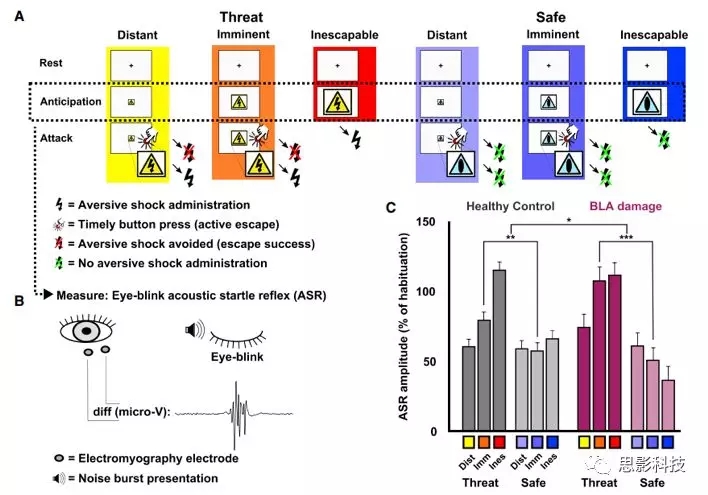
图2 在预期即将到来的可逃避威胁期间,BLA损伤导致ASR过度增强
(三)BLA通过CeA调节脑桥驱动的防御反射
接下来,探究BLA对即将发生的逃避威胁的被动反应的神经通路。通过从CeA到脑干的投射,即分别对于中脑导水管周围灰质(PAG)和脑桥来介导冷冻和威胁增强的惊恐反应。通过将TET与fMRI相结合,在人类受试者中搜索这些区域的活动变化(图3A)。
实验结果
根据之前研究发现,TET引起大脑突显网络的威胁反应(前岛叶,前扣带皮层,丘脑和中脑/ PAG;图3B-3E)。至关重要的是,我们在BLA受损对象的脑桥内观察到一组体素对威胁距离的敏感度明显高于健康对照组(图3F)。这种群体差异是由于相对于遥远的条件,对即将发生的和不可避免的威胁的反应性增加,并且对于迫在眉睫的威胁最为显著(图3F)。因此,类似于惊恐反应,脑干的脑桥区域显示出对即将来临的威胁条件是过度反应的。有趣的是,在健康受试者中,脑桥区域显示出与CeA的威胁相关的功能连接,这些功能连接在BLA损伤的受试者中显著降低(图3G和3H)。该发现表明在BLA损伤的受试者的脑桥中观察到的高反应性是由于CeA的次优调节(suboptimal regulation)。这些结果表明,在快速逃逸准备的情况下,BLA通过参与CeA内的抑制网络的机制导致脑桥驱动的防御反射机制减弱。
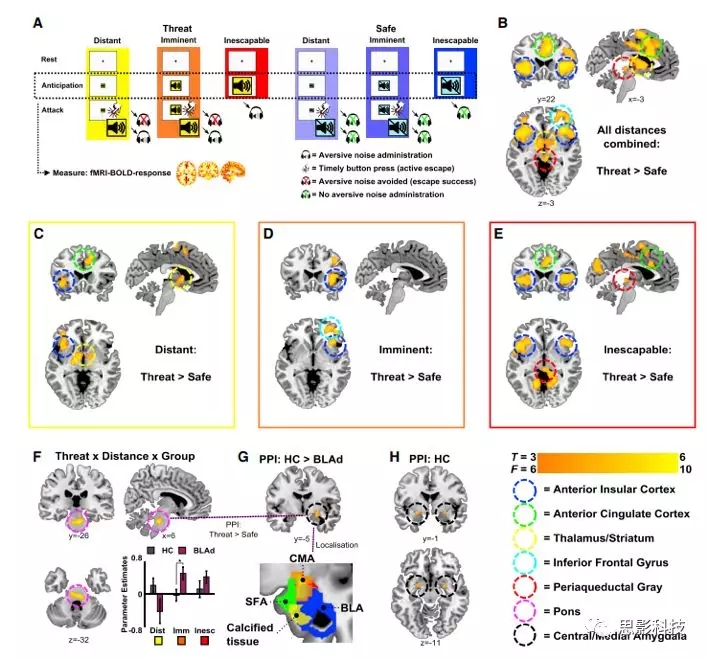
图3 BLA通过CeA调节脑桥驱动的防御反射结果
动物研究
为进一步评估BLA是否对即将发生的威胁响应起作用,文章将人体实验转化为啮齿动物模型,选用具有化学遗传BLA神经元沉默的啮齿动物进行神经生物学实验。
(一)BLA神经元沉默在即将发生威胁时引发被动防御反应机制
作者靶向到大鼠BLA中的谷氨酸能神经元,可将BLA神经元的活性暂时减弱。为大鼠开发了相应版本的TET实验(图4C),扩展单一区域,对不可避免的威胁任务,通过添加相邻的区域进行逃生。在双侧BLA中注射AAV-CamKIIa-hM4D-mCherry后,我们在TET中训练大鼠并评估它们对远处威胁和即将发生威胁的基线逃逸水平能力。作者确定了两个大鼠亚群,以下称为高级逃逸者,称为“HE”,和低级逃逸者,称为“LE”,分类依据是其在遇到迫在眉睫的威胁时的不同行为。与LE大鼠相比,HE大鼠显示出更高的逃避成功能力和对即将来临的威胁的减弱的停滞反应。因此选择HE大鼠并用载体CNO处理它们,使BLA神经元沉默。
实验结果
与载体处理的大鼠相比,具有化学遗传BLA神经元沉默的大鼠在遇到迫在眉睫的威胁时,作者发现其停滞反映增强,并且类似于作者在人BLA钙化中的发现,惊恐反应增强。在远处或不可避免的威胁时,与化学遗传BLA处理的大鼠相比,CNO处理的大鼠显示出相似的停滞水平和惊恐反应增强(图4E和4F)。总之,这些结果表明,当啮齿动物中的威胁迫在眉睫时,BLA损伤者需要减弱停滞和惊吓,并且需要直接快速逃逸的行为。
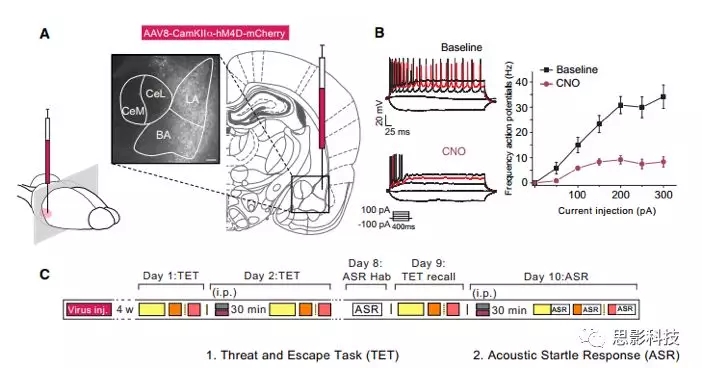
图4.BLA神经元沉默引起即刻威胁时的被动防御反应
(二)OTR +神经元调节对即将发生威胁的主动和被动反应之间的转换
为测试对催产素敏感的神经元在应对即将发生的威胁中的可能作用,作者通过在HE和LE大鼠靶向针对双侧CeL通过药理学控制其活性。在HE大鼠(OTA)中用特定的催产素受体拮抗剂阻断其受体(图6A,6G),有效地将逃避性能降低到迫在眉睫的威胁(图6B)且增强对远处和迫在眉睫的威胁的停滞反映(图6C)。为测试这些神经元的直接激活是否与逃避性能增强和停滞反应减弱,作者测试了LE大鼠,其在基线时表现出低逃逸性能和对即将发生的威胁的高度停滞反应。在该组中注射特定的催产素受体激动剂TGOT(图6D和6G),有效地增强逃避性能并且将停滞反应降低到即将发生而不是遥远的威胁(图6E和6F)。
实验结果
训练后的体外电生理记录显示,与LE和幼稚大鼠相比,HE大鼠的CeL神经元对TGOT的敏感性更高。总之,这些发现进一步证实了OT敏感的CeL神经元在促进对即将发生的威胁的积极反应中起核心作用。

图6.催产素敏感神经元调节对即将发生的威胁的主动和被动反应之间的转换
结论
作者使用多方法研究BLA在被动和主动防御行为中的功能,其中测试了双侧BLA损伤的人和具有化学遗传BLA神经元沉默的啮齿动物。跨物种行为研究表明,当啮齿动物和人类面临迫在眉睫的威胁时,BLA对于快速逃避行为的选择和执行至关重要。通过神经影像学和神经生物学实验,发现BLA在即将来临的威胁下实现快速逃逸的机制,即通过激活特定一组CeA神经元。本研究主要发现,在BLA损伤或沉默后,惊吓威胁增强保持完整,但快速逃避失败。此外,即将到来的逃避威胁期间缺乏惊吓减少,BLA沉默的大鼠表现出适应不良的停滞及逃避性能减弱,表明BLA对于从被动防御转变为主动逃避行为是必要的。相应地,神经影像学数据显示,在即将发生威胁的情况下,BLA受损的人在脑桥脑干中具有异常高的活性,该脑区在启动惊恐反射中起关键作用。对这些人类神经影像数据的探索性功能连接性分析进一步表明BLA通过CeA起作用。
在大鼠中的体外电生理学和体内药理学测量中发现,在成功调节至即将发生但可逃避的威胁之后,从BLA到CeL中的催产素敏感神经元的投射被加强,并且这些神经元在降低停滞反应和促进快速逃逸中起重要作用。这些发现不仅表明BLA与CeL的一致性,对快速逃逸行为至关重要,也表明BLA的这种功能在啮齿动物和人类中是稳定的。
综上所述,作者研究结果与其假设一致:通过抑制停滞反应,BLA投射至CeL中OTR+神经元的增强,可以对迫在眉睫的威胁产生有效的逃避反应。总之,文章的研究结果具有基础和临床相关性,对人类和啮齿动物的进一步生物行为研究是至关重要的。
参考文献:Terburg D, Scheggia D, DelRio R T, et al. The basolateral amygdala is essential for rapid escape: A humanand rodent study[J]. Cell, 2018, 175(3): 723-735. e16.

获取原文:关注“思影科技”公众号,回复“原文”或“培训”,获取原文pdf及补充材料下载链接,同时欢迎浏览我们的培训通知以及数据处理业务介绍。(直接点击下文链接,即可浏览):
第三届动物磁共振脑影像数据处理班 (南京)
第十三届功能磁共振数据处理基础班(重庆)
第十四届功能磁共振数据处理基础班(南京)
更新通知:第八届磁共振脑网络数据处理班(重庆)
第三届脑功能磁共振提高班暨任务态fMRI专题班
第二届脑影像机器学习班(重庆)
第三届脑影像机器学习班(南京)
第七届磁共振弥散张量成像数据处理班(南京)
第四届磁共振ASL(动脉自旋标记)数据处理班(南京)
第二届眼动数据处理班
第一届脑电数据处理入门班 (重庆,全界面)
第十一届脑电数据处理基础班 (南京)
第四届脑电信号数据处理提高班(南京)
更新通知:第五届近红外脑功能数据处理班 (南京)
思影数据处理业务一:功能磁共振(fMRI)
思影数据处理业务二:结构磁共振成像(sMRI)与DTI
思影数据处理业务三:ASL数据处理
思影数据处理业务四:EEG/ERP数据处理
招聘:脑影像数据处理工程师-南京